Dexanabinol
- Seiten mit Skriptfehlern
- Wikipedia:Vorlagenfehler/Vorlage:Cite journal/temporär
- Wikipedia:Vorlagenfehler/Vorlage:Infobox Chemikalie
- Wikipedia:Wikidata-Wartung:PubChem abweichend
- Wikipedia:Wikidata-Wartung:DrugBank fehlt lokal
- Wikipedia:Keine GHS-Gefahrstoffkennzeichnung verfügbar
- Wikipedia:Wikidata-Wartung:CAS-Nummer fehlt lokal
- Seiten mit defekten Dateilinks
- Wikipedia:Vorlagenfehler/Vorlage:Literatur/Parameterfehler
- Wikipedia:Vorlagenfehler/Vorlage:Cite book/temporär
- Cannabinoid
- Arzneistoff
- Phenol
- Cyclohexen
- Allylalkohol
- Dihydropyran
| Strukturformel | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|
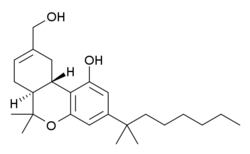
| ||||||||||
| Allgemeines | ||||||||||
| Freiname | Dexanabinol | |||||||||
| Andere Namen |
| |||||||||
| Summenformel | C25H38O3 | |||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||
| ||||||||||
| Arzneistoffangaben | ||||||||||
| Wirkstoffklasse |
Antiemetikum | |||||||||
| Eigenschaften | ||||||||||
| Molare Masse | 386,57 g·mol−1 | |||||||||
| Sicherheitshinweise | ||||||||||
| ||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||
Dexanabinol (HU-211) ist ein synthetisches Cannabinoid, welches nicht an CB1- und CB2-Rezeptoren bindet.
Chemie
Dexanabinol ist das Enantiomer von HU-210, einem sehr potenten Cannabinoid. Strukturell gesehen ist es das Spiegelbild des Seitenketten-Homologon des THC-Metaboliten 11-Hydroxy-Δ9-tetrahydrocannabinol.
Die ursprüngliche Synthese von HU-211 basiert auf einer säure-katalysierten Kondensation von (+)-Myrtenol und 1,1-Dimethylheptylresorcinol (3,5-Dihydroxy-1-(1,1-dimethylheptyl)benzol).[2]
Es wurde in der Arbeitsgruppe von Raphael Mechoulam an der Hebräischen Universität in Jerusalem entwickelt.[3] HU-211 bindet nicht an bekannte Cannabinoid-Rezeptoren, aber an NMDA-Kanäle und wurde deshalb als potentielles Medikament für Schädel-Hirn-Trauma getestet, war aber in klinischen Studien nicht effektiver als Placebo.[4]
Literatur
- Razdan, K.: The Total Synthesis of Natural Products. Hrsg.: John Apsimon. Wiley Interscience, 1981, ISBN 978-0-471-05460-3, The Total Synthesis of Cannabinoids, S. 245.
Einzelnachweise
- ↑ Dieser Stoff wurde in Bezug auf seine Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- ↑ R. Mechoulam, N. Lander, A. Breuer, J. Zahalka: In Synthesis of the Individual, Pharmacologically Distinct, Enantiomers of a Tetrahydrocannabinol Derivative. Tetrahedron: Asymmetry 1990, 5, 315-318.
- ↑ Zeltser R, Seltzer Z, Eisen A, Feigenbaum JJ, Mechoulam R: Suppression of neuropathic pain behavior in rats by a non-psychotropic synthetic cannabinoid with NMDA receptor-blocking properties. In: Pain. 47. Jahrgang, Nr. 1, Oktober 1991, S. 95–103, PMID 1663228.
- ↑ Maas AI, Murray G, Henney H, et al.: Efficacy and safety of dexanabinol in severe traumatic brain injury: results of a phase III randomised, placebo-controlled, clinical trial. In: Lancet Neurol. 5. Jahrgang, Nr. 1, Januar 2006, S. 38–45, doi:10.1016/S1474-4422(05)70253-2, PMID 16361021.
Weblinks
- Material Safety Data Sheet HU-211 (PDF-Datei; 19 kB)
- HU-211 als Produkt bei Cayman Chemical