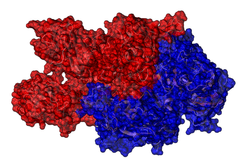
Blutgerinnungsfaktor VIII
| Gerinnungsfaktor VIII | ||
|---|---|---|
| Bänder-/Oberflächenmodell von Faktor VIII (ohne B-Kette) nach PDB 3CDZ. Die leichte Kette ist rot, die schwere blau markiert. | ||
| Vorhandene Strukturdaten: 1cfg, 1d7p, 1iqd, 1fac, 2r7e, 3cdz | ||
| Eigenschaften des menschlichen Proteins | ||
| Masse/Länge Primärstruktur | 265 kDa/2332 AS | |
| Kofaktor | von-Willebrand-Faktor | |
| Bezeichner | ||
| Gen-Namen | F8; AHF; DXS1253E; F8 protein; F8B; F8C; FVIII; HEMA | |
| Externe IDs | OMIM: 306700 UniProt: P00451 MGI: 88383 | |
| Arzneistoffangaben | ||
| ATC-Code | B02BD02 | |
| DrugBank | DB00025 | |
| Verschreibungspflicht | ja | |
| Vorkommen | ||
| Homologie-Familie | Gerinnungsfaktor 5 | |
| Übergeordnetes Taxon | Euteleostomi | |
Blutgerinnungsfaktor VIII (F8), auch Antihämophiles Globulin A, ist ein Glykoprotein und ein Gerinnungsfaktor bei Wirbeltieren. Ein Mangel des Gerinnungsfaktors beim Menschen führt zur Hämophilie A (sog. Bluterkrankheit). Ursache ist immer eine Mutation im F8-Gen, das für den Faktor VIII codiert. Eine intravenöse Zufuhr dieses Blutgerinnungsfaktors ist daher die einzige Therapie für Bluterkranke. Bis Ende der 1980er-Jahre wurde Faktor VIII ausschließlich aus gespendetem humanem Blutplasma gewonnen, heute stehen auch mehrere gentechnisch hergestellte Präparate zur Verfügung.
Biosynthese
Der Syntheseort des Faktor VIII ist noch nicht vollständig geklärt. Als Syntheseort wird neben der Leber auch Endothel diskutiert. Der Abbau findet in Leber und Niere statt.[1][2][3]
Das F8-Gen umspannt 187000 Basenpaare in 26 Exons. Die transkribierte mRNA ist 9029 Basen lang und wird in ein Protein mit 2351 Aminosäuren translatiert, von dem durch posttranslationale Modifikation weitere 19 Aminosäuren entfernt werden.[4]
Das Faktor VIII-Molekül wird an 31 Aminosäureseitenketten mit komplexen Zuckermolekülen modifiziert (25 x N-Glykosylierung, 6 x O-Glykosylierung), die Aminosäurekette wird schließlich durch spezifische Proteasen an zwei Stellen geschnitten. Das fertige Molekül besteht aus zwei Ketten, einer 200 kDa großen schweren Kette und einer 80 kDa großen leichten Kette.
Biologische Funktion
Faktor VIII, zusammen mit Calcium und Phospholipiden (die bei Verletzungen entstehen) sind die Kofaktoren für Faktor IXa, der notwendig ist, um Faktor X zu aktivieren. Dieser Reaktionsschritt ist essentiell für die Blutgerinnung, denn Faktor Xa aktiviert im Komplex mit Faktor Va Prothrombin zu Thrombin und dieses setzt Fibrin aus Fibrinogen frei.
Pharmakologie
Die Substitution von Faktor VIII (intravenöse Applikation) ist für Hämophilie A-Patienten die Therapie der Wahl. Bis zum Jahr 1992 wurde Faktor VIII ausschließlich aus humanem Blutplasma hergestellt. Inzwischen stehen neben den aus Plasma gewonnenen auch gentechnisch erzeugte Faktorkonzentrate wie Octocog-alfa zur Verfügung.
Herstellung aus Plasma
Faktor VIII wird aus humanem Plasma durch Kältefällung (Kryopräzipitation) gewonnen und anschließend chromatographisch gereinigt. Ein wichtiges Ziel in der Produktion ist die Inaktivierung potentieller Pathogene (z.B. Viren). Neben der Selektion der Spender und dem Test des verarbeiteten Plasmas gehören inaktivierende Produktionsschritte wie Lösungsmittel/Detergenz-Behandlung (S/D-Verfahren, Inaktivierung umhüllter Viren), Hitze und/oder Nanofiltration zum heutigen Sicherheitsstandard.
Octocog-alfa
Octocog-alfa (INN) ist rekombinant hergestellter humaner Faktor VIII, der als Arzneistoff identische Anwendungsgebiete zum aus Plasma hergestellten Faktor VIII hat. Chemisch unterscheidet er sich nur unwesentlich von diesem. Die folgenden Ausführungen gelten daher auch für Octocog-alfa.
Octocog-alfa wird nicht aus humanen Blutplasma extrahiert, sondern mittels rekombinanter DNA-Technologie hergestellt: Es wird von einer Zelle produziert, in die ein Gen eingeschleust wurde, das sie zur Expression des humanen Gerinnungsfaktors VIII befähigt (siehe auch Pharmazeutische Biotechnologie).
Dosierung, Art und Dauer der Anwendung
Die Dosierung und Häufigkeit der Anwendung richtet sich danach, ob Faktor VIII zur Behandlung von Blutungen, zur Prophylaxe von Blutungen oder im Rahmen eines chirurgischen Eingriffes eingesetzt wird. Die Dosierung wird darüber hinaus abhängig vom Schweregrad der Blutung und der Art des chirurgischen Eingriffes angepasst.
Gegenanzeigen
Kontraindiziert sind alle Analgetika mit thrombozytenaggregationshemmender Wirkung, besonders Acetylsalicylsäure. Indiziert sind beispielsweise Dextropropoxyphen, Tilidin + Naloxon, Pentetocin, Buprenorphin, Paracetamol, Diclofenac.
Unerwünschte Wirkungen
Patienten mit Hämophilie A können Antikörper (Inhibitoren) gegenüber Faktor VIII bilden. Ein Antikörper ist ein Protein, das vom Körper aufgrund seines natürlichen Schutzmechanismus als Reaktion auf unbekannte Stoffe gebildet wird. Die Antikörperbildung richtet sich gegen den zugeführten Gerinnungsfaktor und resultiert in einer kompletten oder partiellen Inaktivierung des Faktors. Als Folge kommen Blutungen trotz Anwendung üblicher Faktordosierungen nicht oder verzögert zum Stillstand – die so genannte „Hemmkörperhämophilie“.
Patienten mit Hemmkörpern werden nach ihrem Hemmkörpertiter als „Low Responder“ und „High Responder“ charakterisiert. Hemmkörper können sich spontan zurückbilden, bei Low Respondern eher als bei High Respondern. Die Behandlung der akuten Blutung ist symptomatisch. Die kausale Behandlung besteht in der Elimination oder Reduktion der Hemmkörper durch Erzeugung einer Immuntoleranz (Immuntoleranzinduktion, ITI) und sollte immer angestrebt werden. Sowohl bei der symptomatischen Behandlung der akuten Blutung als auch bei der Hemmkörperelimination müssen Faktorenkonzentrate hoch dosiert verabreicht werden.
Bei einer allergischen Reaktion nach Infusionsbeginn muss die Infusion gestoppt und auf ein anderes Präparat gewechselt werden. Bei einer anaphylaktischen Reaktion gelten die üblichen Notfallbehandlungsmaßnahmen.
In den achtziger Jahren kam es durch verunreinigtes Spenderblut bei Hämophilen weltweit zu HIV- und Hepatitis-Infektionen aufgrund von Unkenntnis aber auch Fahrlässigkeit und z. T. sogar Profitsucht.[5] Dies wurde in einigen Ländern als "Blutskandal" bekannt.[6]
Einzelnachweise
- ↑ Charité: Parameterbestimmung im Blut
- ↑ Blutgerinnungsfaktor VIII. In: {{Modul:Vorlage:lang}} Modul:Multilingual:149: attempt to index field 'data' (a nil value). (englisch).
- ↑ AOK über Faktor VIII Blutwert
- ↑ ENSEMBL-Eintrag
- ↑ Produktinfo Advate
- ↑ Aids scandals around the world BBC News, 9. August 2001