GM-CSF
- Wikipedia:Vorlagenfehler/Vorlage:Cite journal/temporär
- ATC-L03
- Wachstumsfaktor
- Zytokin
| GM-CSF | ||
|---|---|---|
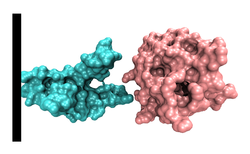
| Oberflächenmodell mit Cytokinrezeptor-Untereinheit beta, nach PDB 3CXE | ||
| Eigenschaften des menschlichen Proteins | ||
| Masse/Länge Primärstruktur | 127 Aminosäuren | |
| Sekundär- bis Quartärstruktur | Monomer | |
| Bezeichner | ||
| Gen-Name | CSF2 | |
| Externe IDs | OMIM: 138960 UniProt: P04141 CAS-Nummer: 83869-56-1 | |
| Arzneistoffangaben | ||
| ATC-Code | L03AA09 | |
| DrugBank | DB00020 | |
| Wirkstoffklasse | Immunstimulans | |
| Verschreibungspflicht | ja | |
| Vorkommen | ||
| Übergeordnetes Taxon | Säugetiere[1] | |
GM-CSF (von engl. Granulocyte macrophage colony-stimulating factor) ist ein Glykoprotein, das in Säugetieren als Cytokin wirkt.
Es wird im Körper von Zellen des Immunsystems und des Endothels ins Blut abgegeben. In Kultur kann er die Differenzierung von Vorläuferzellen des Knochenmarks in Granulozyten und Macrophagen bewirken.[2] In Tieren ist eine Differenzierung in Granulocyten und Macrophagen auch ohne GM-CSF möglich, wenn auch deutlich weniger entsprechende Zellen gebildet werden.[3]
GM-CSF ist auch Teil der Immunantwort auf Antigene und Mitogene.
Offenbar handelt es sich bei GM-CSF als T-Zell-Zytokin um einen notwendigen Faktor für die Entstehung von autoimmunen Entzündungsreaktionen wie sie bei der Multiplen Sklerose vorkommen. Es begünstigt dabei außerdem die Einwanderung von gewebeschädigenden Fresszelle in das Zentrale Nervensystem. Im Tierversuch konnte nachgewiesen werden, dass eine Neutralisation von GM-CSF den Ausbruch der EAE, einem Tiermodell der Multiplen Sklerose, verhindert und bei bereits erkrankten Tieren zur Heilung führt. Dieses Neutralisationsverfahren wird derzeit bei an Multipler Sklerose und rheumatoider Arthritis erkrankten Personen getestet.[4][5]
Arzneistoff
Rekombinant hergestellter GM-CSF ist als Sargramostim und Molgramostim Bestandteil von Arzneimitteln zur Immunstimulation; die Hauptanwendung liegt bei der Behandlung von Neutropenie nach Radiotherapie. Eine Variante des GM-CSF konnte mit einem Risiko für atopisches Asthma assoziiert werden.[6][7]
Dendritische Zellen für die Immuntherapie werden üblicherweise aus Monozyten des Patienten durch Kultur in GM-CSF und IL-4 erhalten. In der Kombinations-Immunotherapie wird GM-CSF zusammen mit immunisierenden Agentien mit Erfolg verabreicht.[8][9][10]
Einzelnachweise
- ↑ Homologe bei OMA
- ↑ Hamilton JA, Anderson GP: GM-CSF Biology. In: Growth Factors. 22. Jahrgang, Nr. 4, Dezember 2004, S. 225–31, doi:10.1080/08977190412331279881, PMID 15621725.
- ↑ Hibbs ML, Quilici C, Kountouri N, Seymour JF, Armes JE, Burgess AW, Dunn AR: Mice lacking three myeloid colony-stimulating factors (G-CSF, GM-CSF, and M-CSF) still produce macrophages and granulocytes and mount an inflammatory response in a sterile model of peritonitis. In: J. Immunol. 178. Jahrgang, Nr. 10, Mai 2007, S. 6435–43, PMID 17475873.
- ↑ Codarri, L., Gyülveszi, G., Magnenat, L., Hesske, L., Fontana, A., Suter, T.,Becher, B.: RORgt drives production of the cytokine GM-CSF in helper T cells, which is essential for the effector phase of autoimmune neuroinflammation. In: Nature Immunology. April 2011, doi:10.1038/ni.2027, PMID 21516112.
- ↑ "Für Immunangriffe bei Multipler Sklerose braucht es GM-CSF" von journalmed.de - abgerufen am 1. Mai 2011
- ↑ UniProt P04141
- ↑ H. Ibelgaufts/COPE: GM-CSF
- ↑ Tawab A, Fan Y, Read EJ, Kurlander RJ: Effect of ex vivo culture duration on phenotype and cytokine production by mature dendritic cells derived from peripheral blood monocytes. In: Transfusion. 49. Jahrgang, Nr. 3, März 2009, S. 536–47, doi:10.1111/j.1537-2995.2008.02020.x, PMID 19243546.
- ↑ Seo SH, Han HD, Noh KH, Kim TW, Son SW: Chitosan hydrogel containing GMCSF and a cancer drug exerts synergistic anti-tumor effects via the induction of CD8+ T cell-mediated anti-tumor immunity. In: Clin. Exp. Metastasis. 26. Jahrgang, Nr. 3, 2009, S. 179–87, doi:10.1007/s10585-008-9228-5, PMID 19082918.
- ↑ Fong L, Kwek SS, O'Brien S, et al.: Potentiating endogenous antitumor immunity to prostate cancer through combination immunotherapy with CTLA4 blockade and GM-CSF. In: Cancer Res. 69. Jahrgang, Nr. 2, Januar 2009, S. 609–15, doi:10.1158/0008-5472.CAN-08-3529, PMID 19147575.